败血症是一种由病原微生物侵入血液循环系统引发的全身感染性疾病。病原体耐药性和宿主免疫系统的过度激活是败血症治疗过程中亟待解决的难题。尽管抗生素是目前临床治疗败血症的主要手段,然而抗生素的滥用导致多重耐药细菌(MDR)甚至是超级细菌的出现进一步加大了败血症治疗的难度。纳米抗菌药物在对抗MDR细菌和调节炎症方面表现出广泛的应用潜力,但其在血液循环过程中可能导致代谢困难和潜在的毒副作用,以及纳米材料对细菌捕获能力方面存在不足(尤其是在败血症的早期,细菌浓度非常低的情况下)是阻碍其临床应用的两个关键问题。因此,开发具有高效细菌捕获能力和可清除性能的纳米抗菌材料对于治疗败血症至关重要。

光动力疗法(PDT)由于其无耐药性、全身毒性低、副作用小等优势显示出广泛的应用前景,具有体外血液光动力消毒治疗败血症的潜力。西南交通大学生命分析技术与材料团队致力于光敏抗菌药物(PS)的开发,在前期工作中,提出了质膜靶向多模式联合治疗策略解决细菌耐药性。针对传统阳离子抗菌药物潜在的毒性和提高光敏药物在复杂场景中的临床应用潜力,通过对PS电荷调控实现对革兰氏阳性菌(G+)、革兰氏阴性菌(G-)和肿瘤细胞选择性结合和分级分类治疗(ACS Appl. Mater. Interfaces, 2023, 15, 17433−17443; Chem. Eng. J. 2023, 454, 140189. );利用噬菌体对细菌的高度选择性,将光敏剂通过共价键修饰在噬菌体得到功能化噬菌体,实现对临床败血症样品60 min的精准快速检测(Adv. Mater. 2023, 35, 2208578);通过提高光敏剂与质膜的结合性能,不仅有效提高生物膜渗透性,且与生物膜形成(如定植、黏附、迁移等)、信号转导系统(如群体感应、双组分系统、毒力因子等)和耐多药外排相关的多种蛋白质结合,进一步联合光动力和噬菌体鸡尾酒疗法协同治疗,避免耐药性的产生(Adv. Mater. 2023, DOI:10.1002/adma.202309797; Adv. Sci. 2023, DOI: 10.1002/advs.202207736;Adv. Mater. 2023, 35, 2208578)。
基于以上研究,该团队利用磁性纳米颗粒(NPs)独特的病原体富集与捕获能力,以及磁性分离特性,成功规避了与血液循环和代谢相关的问题,制备了一种聚集诱导发光光敏剂武装的磁性纳米颗粒,Fe3O4@SH@TBTCP-PMB,用于治疗败血症。磁性NPs和PDT的协同作用为败血症治疗提供了有效的解决方案,为进一步解决光敏药物或抗菌材料在败血症治疗过程中对耐药细菌捕获能力不足以及长期血液循环和代谢困难等问题提供理论指导。该工作以“Aggregation-Induced Emission Photosensitizer-Armored Magnetic Nanoparticles for Sepsis Treatment: Combating Multidrug-Resistant Bacteria and Alleviating Inflammation”为题发表在《Advanced Functional Materials》上。西南交通大学为本论文的通讯单位,文章第一作者是西南交通大学博士生王嘉莉,通讯作者是吴明雨和封顺教授。该研究得到国家自然科学基金委的支持(22177094,22174117)。
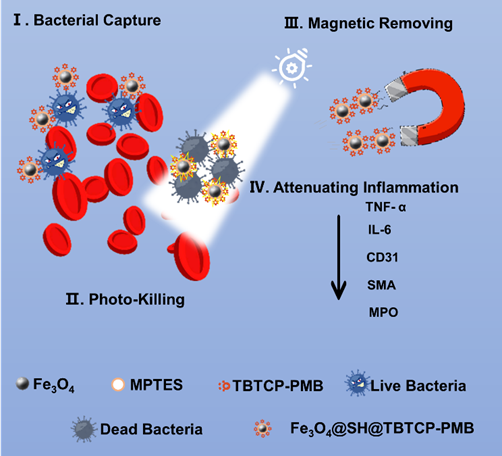
图1 磁性纳米颗粒的制备和AIE PS武装磁性纳米颗粒进行败血症治疗的过程。
【磁性纳米颗粒的表征及光物理性质】
充分利用磁性纳米颗粒和AIE PS的独特属性,开发AIE PS武装的磁性纳米颗粒, Fe3O4@SH@TBTCP-PMB(图1)。这种创新的纳米复合物具有显著的超顺磁性,高效产生ROS的能力,和带正电的特性(图2),阳离子光敏剂增强了磁性纳米材料通过静电相互作用捕获细菌的能力,磁分离的性能可以有效规避光敏剂通过血液循环导致的潜在毒性。
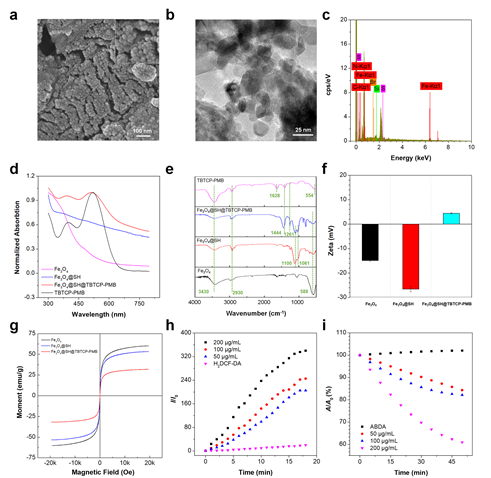
图2 Fe3O4@SH@TBTCP-PMB的表征和光物理性质
【磁性纳米颗粒的细菌捕获和富集能力】
Fe3O4@SH@TBTCP-PMB在不同的环境中(缓冲溶液PBS,水,细胞培养基DMEM,血清和血液)对革兰氏阳性菌具有超强的捕获能力。在短短1小时内,即使在低细菌浓度下,也能以超过80%的富集效率捕获革兰阳性细菌。(图3)。
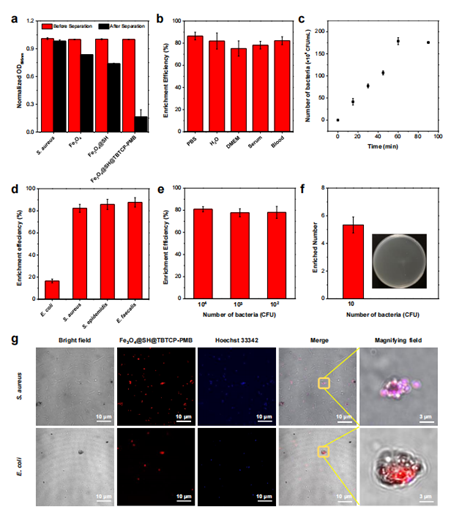
图3 Fe3O4@SH@TBTCP-PMB对细菌捕获和富集能力
【磁性纳米颗粒体外抗菌作用】
磁性纳米颗粒对革兰氏阳性菌(金黄色葡萄球菌、耐甲氧西林的金黄色葡萄球菌(MRSA)、表皮葡萄球菌和粪肠球菌)表现出优异的抗菌效果。100 µg mL-1 的Fe3O4@SH@TBTCP-PMB能够有效杀灭超过99.9%的MRSA,证明Fe3O4@SH@TBTCP-PMB对革兰氏阳性MDR菌表现出良好的选择性和杀灭能力(图4)
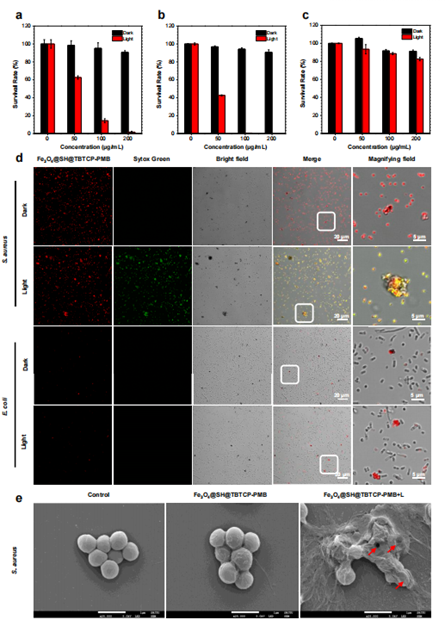
图4 Fe3O4@SH@TBTCP-PMB抗菌性能研究
【磁性纳米颗粒体内抗菌作用】
基于Fe3O4@SH@TBTCP-PMB在体外表现出的卓越细菌捕获、磁分离特性和优异的抗菌性能,进一步通过建立耐甲氧西林金黄色葡萄球菌(MRSA)感染的小鼠败血症模型来研究Fe3O4@SH@TBTCP-PMB的体内抗菌效果。研究表明,在白光照射下,Fe3O4@SH@TBTCP-PMB不仅具有优异的杀菌效果,而且可以通过调节细胞因子、降低粘附分子表达、调控氧化应激水平从而缓解炎症,有效治疗小鼠败血症,提高存活率(图5和图6)。
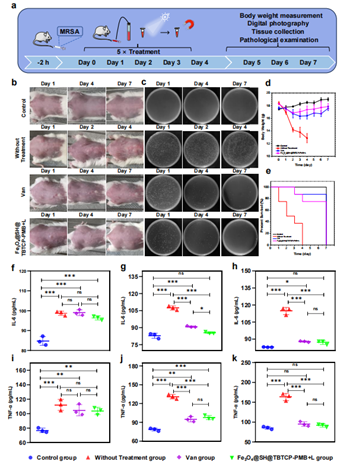
图5 Fe3O4@SH@TBTCP-PMB用于治疗败血症
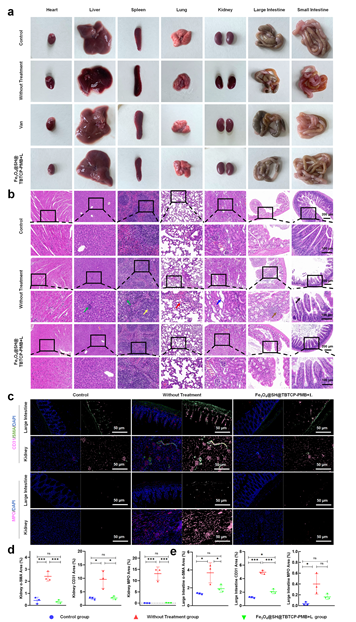
图6 败血症小鼠不同治疗组的组织学分析
【小结】
该研究制备了一种阳离子AIE光敏剂武装的磁性颗粒,即Fe3O4@SH@TBTCP-PMB,用于治疗败血症。阳离子光敏剂具有高效的ROS生成效率和优秀的细菌结合能力,这些特性与Fe3O4的磁捕获和磁分离特性协同作用,使得Fe3O4@SH@TBTCP-PMB在低浓度下能够迅速捕获革兰氏阳性细菌,并在光照条件下显著灭活耐药细菌。AIE PS功能化的磁性NPs展现出广泛的应用潜力,通过抑制炎症因子和细胞因子以减少炎症反应,有助于改善多器官功能障碍,恢复先天免疫防御系统,为克服多药耐药细菌引发的血液感染提供了有效的治疗策略。
原文链接:
https://doi.org/10.1002/adfm.202312162
Wang, J.-L., Chen, Y., Song, J.-X., Guo, B.-W., Xia, F.-W., Wan, Y., Wu, W.-X., Zhang, C., Feng, S., Wu, M.-Y., Aggregation-Induced Emission Photosensitizer-Armored Magnetic Nanoparticles for Sepsis Treatment: Combating Multidrug-Resistant Bacteria and Alleviating Inflammation. Adv. Funct. Mater. 2023, 2312162. DOI: 10.1002/adfm.202312162
